화학1 산,염기 관련된 문제 질문드려요~


위에 문제 질문드려요~
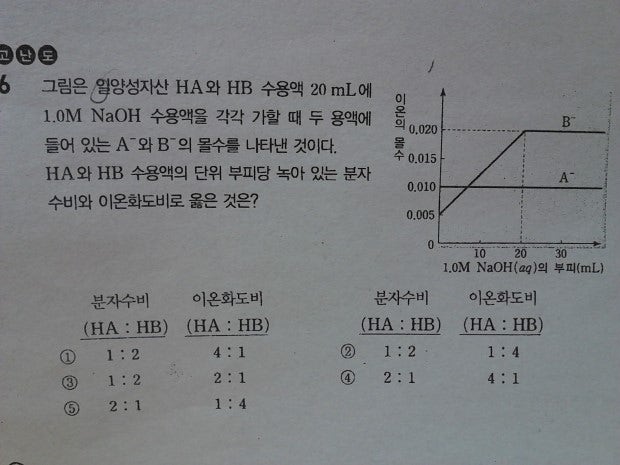
1. B- 이온수가 NaOH의 넣어준 양과 무슨 관련이 있는거죠? 구경꾼이온은 반응에 참여 안하니까 넣어준 HB 20ml 안에 있는 B- 이온수는 변함이 없을것 같은데 증가하다가 일정하네요..
즉, 답지에선 A-이온이 강산의 짝염기이고, B-이온은 약산의 짝염기라서 위 모양의 그래프가 나왔다는데 강산 혹은 약산의 짝염기라는것과 NaOH를 넣어줌에 따라 A-, B-이온수의 변화와 무슨 관계가 있는지 궁금합니다~
2. 이온화도를 비교하는 부분에서, 이온화도= 이온화된 용질의 몰수/용질의 전체 몰수 아닌가요..?
근데 그래프 상에서 녹아있는 이온수와 전체 이온수에 대한 정보를 어디서 찾을수 있나요?;
0 XDK (+0)
유익한 글을 읽었다면 작성자에게 XDK를 선물하세요.
-
안녕하세요:) 원서철 눈팅하다가 정보를 좀 얻고자하여 글을 작성하게 되었습니다!...
-
낙지 칸수 보면서 인하대 넣으려고 하는데 6칸이었던 다른 과들이 일주일도 안돼서...
-
이관데 이번에 국어가 높게나와서 경제 안정권이던데 가볼까 생각중 물론 맘에안들면...
-
부산대 전과 3
부산대 전과 또는 복전 하기 어렵나요?
-
오랜만에 오르비에 들어왔는데 건국대 전과나 다전공을 궁금해하시는 분들이 계셔 정보...
-
전남대 여수캠에서 광주캠으로 전과하기 vs 재수하기 11
어떤게 더 나아보이나요.. 부모님은 여수캠가서 전과 하라고 하시고.. 저는 재수를...
-
에타에 전과 관련 글 많이 올라오나요...? 기계공 오늘 붙으면 전자공 전과 목표로...
-
먼저 글을 쓰기 앞서 음악 틀어놓고 가세요. 0:01 소크나 / 2:35 보헤미안...
-
중대 공대 전과 4
중대 공대에서 공대로 전과 많이 어려울까요?ㅠㅠㅜ
-
경희대 전과 문과->이과 가능?
-
중앙대학교 간호학과에 갔다가 전과하게되면 전과한 과에서 교직이수도 할 수 있나요?
-
ㅈㄱㄴ 어떻게 가능한가요?
-
ㅈㄱㄴ
-
중앙대 전과 6
중앙대 에너지시스템공학부에서 화학신소재공학부로 전과하려고 또 글을 씁니다.......
-
중앙대 에너지시스템공학부인데 중앙대 화학신소재공학부를 2학년때부터 복전하면 얼마나 힘들까요?
-
내가 원하는 과가 있는 대학이 있고 내가 원하는 과는 없지만 높은 대학이 있을 때...
-
문과인데요 정시 원서 접수 관련해서 질문이 있어서요 내가 원하는 과가 있는 대학이...
-
제가 중앙대 에너지시스템공학부를 붙어서 가게 되었습니다. 그런데 대학에 가서...
-
중앙대 전과 2
중앙대 에시공인데 화학신소재로 전과하고 싶습니다. 전과 잘 되는 편인가요?
-
교과로 건축갈 성적은 안되서 안전빵으로 지거국 낮은과에 교과 쓰려고 합니다
-
반수했다가 실패해서 복귀하면 2학년때 전과나 복전은 불가능한가요? 0
1-2를 휴학할텐데 그럼 2학기를 다시 듣고나서 복전이나 다전 할 수...
-
만약 둘 다 붙는다면, 홍익대 기시디를 갈까요, 아니면 건국대 낮은과 들어가서...
-
문과로 전과한 이과재수생입니다 노베이스 재수생이라서 ..ㅠㅠ 조언좀부탁합니다 최소...
-
중대 인문대에서 경영경제대, 사회과학대로 전과하는 사람만 50명에 육박하네요....
-
문과에서 이과로 7
바꿔서 재수하는거는 너무 도박인가요.. 만약에 그러면 재종반은 못들어가는건가요??
-
문과생 이과로 전과해서 의대갈려구 하는데 매우 고난하겠죠...? ㅠ 12
이번수능 국어 말아먹고 수학 2개틀 영어 90점대 1등급 탐구 5050인데 이과로...
-
전과목적으로 사환시쓴다고 했더니 진학당담쌤이 제일낮은과는 전과하기너무빡세다고...
-
한양대 논술 원자력 써서 원자력->기계 전과 하려고 하는데 할 만한가요?
-
이과 수탐 노베 문과로 전과하면 연고(고연)대 가능? 9
대강 24275인데 가능?
-
진짜로 문과로 전과할까 13
난이도 국어 공통 문과수학 <<< 이과수학 영어 공통 사탐 <<<<< 과탐 (제...
-
이과에서 문과 0
2017 수능 끝나고 재수를 결정한 재수생입니다. 중학교 때부터 무조건 간호사가...
-
아주대는 가게된다면 소프트나 사이버보안으로 전과신청을할려구하는데요 중학교때부터 꿈이...
-
문과 취업 2
저는 복수전공하면 취직할때 상관없다고 생각했는데 본전공하고 차이 많이두나요? 그리고...
-
현재 한양대 파이낸스경영학과에 재학중인 이제 2학년 되는 학생입니다. 제 원래 꿈이...
-
문과에서 꿈이나 진로가 명확하지 않다면 전과가 답인가요?? 0
지금 예비 고3입니다 그냥 살면서 주위 사람들이 전부 넌 문과체질이라 하고 저도...
-
안녕하세요. 지금 학교에서는 축제준비며 여러가지로 바쁜 와중에 주말이어서 조금...
-
예를들어 전정공 -> 기계라던지
-
생1:작년수능 6 > 6평 5 > 9평 3 > 올해 수능 1 (원점수 47점)...
-
올해 수능을 평소보다 많이 못봐서 재수를 하게 됐는데 제가 원래 과학을 좋아하고...
-
노베가 개념부터 김지혁 풀커리로 타는 것 어떻게 생각하세요?
-
이과로 전과 할건데 메가스터디에서 교재 사서 풀어볼만한거 추천좀요. 2
이과로 전과 할건데 메가스터디에서 교재 사서 풀어볼만한거 추천좀요.
-
지금 공대준비중이기는한데, 수학/과학공부를 해보니 너무 적성에...
-
문과수학 모평 및 수능 항상고정 1등급이었던 학생인데2월부터 이과수학 시작해서 하루...
-
예체능 과탐->사탐 10
원래 이과인 예체능입니다. 과탐 지1 생1 했는데 지구과학은 보지도않았고 생명은...
-
이과 문과 선택 2
문관데 이과로 전과하고 싶어요.. 수학 진짜 못해요 그런데 코스메틱 (화장품 쪽...
-
하고싶은일들이 문과쪽일이기도하고.. 현역 수B 특히 기벡이 진짜 해도해도...
-
물론 딱 뭐가더쉽다 어렵긴하지만.. 그래도요. (전과는 문이과 말고 대학교과) (중대에용)
-
작년, 그니까 16수능대비 강의 들어도 괜찮을까요? 3
제가 올해 전과해서 과탐 문외한이다보니, 일단 1월 전까지 개념강의 한 바퀴 돌릴...
-
제마에서도 썼던 글이지만.. 15수능을 마지막으로 보고 15학번으로 대학에 들어간...





































헐 이거 화학1으로 내려왔나요? ㄷㄷ
화학2 내용이었나요? ㅋㅋ;
어쩐지 어렵더라구요 ㅠㅠ
1. 네 이 부분이 밑에 말씀드린 중화적정과 더불어 가장 중요한, 심화 문제 풀이에 있어서 핵심적인 아이디어가 되는 부분입니다.
우선 B-이온은 구경꾼 이온이지만 다른 이온반응의 구경꾼 이온과 다르다는 사실을 매우 유념하여야 합니다
그 이유는 HB의 경우 '약산'입니다.
약산은 처음에 이온화가 대부분 되어있지 않습니다. 예를 들면 HB 1몰 있을때 H+ B-는 0.1몰 있다고 해보죠
여기서 H+가 들어온 OH-와 이온화가 됩니다
그러면 H+는 사라지죠 (B- 0.1몰은 그대로 있어요)
이때 다시 HB가 0.1몰 만큼 이온화가 됩니다
원래 있던 B-와, 새로 이온화된 B-가 합쳐져서 0.2몰로 양이 늘어나게 됩니다.
이런 과정이 중화점까지 쭉 이어지게 되있어요
그럼 HB가 약산인것을 어떻게 아느냐?
위의 아이디어를 이해하고 외워두면
위의 그래프처럼 B-의 이온이 증가하는 그래프를 보고 약산이라고 결론을 내릴수있어요
반드시 이해하고 암기하셔야할 사항입니다.
반면에 HA는 강산입니다
왜냐하면 만약에 약산이라면 위의 과정을 겪을테고, 아니니까 강산입니다
즉 처음부터 모든 HA가 이온화되어있습니다.
2. 말씀하신 부분 이온화도= 이온화된 용질의 몰수/용질의 전체 몰수 은 맞는내용입니다.
여기에서 이온화된 용질의 몰수와 용질의 전체 몰수는 사고를 통해서 찾아내야 합니다
처음의 이온화된 용질의 몰수가 0.010 mol / 0.005 mol 임은 바로 알수있습니다.
조금 헷갈릴수가 있어요. 막 이렇게 저렇게 복잡하게 생각할수있거든요.
아직은 중화가 전혀 되지 않은 상태이기 때문에, 위의 그래프의 몰수 (이온화된 몰수)를 통해서 비교를 할수가 있습니다.
그럼 그때 '용질의 전체 몰수'는 어떻게 알 수 있을까요?
nMV = n'M'V' 공식을 보셨을 겁니다. 그것을 사용하셔서 구하시면 됩니다
밑의 문제에서 말씀드렸듯이 약산이라고 해도 지속적으로 이온화가 일어나기 때문에
전체 몰수를 비교할때 약산/강산에 상관없이 위의 공식을 사용할수 있습니다.
그러면 B의 경우 중화점까지 넣어준 NaOH의 부피가 20mL입니다
그러므로 1 * 20 = 1 * 20 이므로 B의 농도 (이온화/이온화 안된걸 포함한 전체 용질의 농도)는 1M이 됩니다.
전체 용질의 몰수를 구해야 하므로 농도 x 부피 = 1 * 0.02 = 0.02 mol 입니다.
여기에서 A의 경우는 조금 다릅니다. 위의 그래프로는 중화점을 찾을수가 없어요
그러면 좀더 생각을 해봐야 합니다
A는 강산이므로 처음에 모든 용질이 이온화가 됩니다
그러므로 처음의 용질 몰수는 0.01 mol 입니다.
A의 이온화도 0.01/0.01 = 1 입니다 (강산이므로)
B의 이온화도 0.005/0.02 = 0.25 입니다
그러므로 이온화도의 비는 4 : 1 입니다.
이온화도 = 이온화된 용질의 몰수/ 용질의 전체 몰수 에서요~
분자의 이온화된 용질의 몰수는 맨처음 NaOH를 넣지 않은 상태에서의 몰수를 말하는 건가요?
그렇다면 이온화도를 구할때 B- 이온의 몰수가 맨 처음엔 0.005 였다가 중화점에서 0.02 이므로 0.005/0.02 이렇게 구해도 되는건가요?
네 결과적으로 보면 맞다고 해야 겠네요
B-이온이 중화점에 이르면 다 이온화가 되고,
H가 1가 산이므로 HB 한분자당 B-이온이 1개 나오므로 그렇게 구해도 됩니다.
2가 산일 경우에는 다르게 해야겠지요